Lista ozbiljnih nuspojava
HALMED objavio novi popis ozbiljnih nuspojava kodiranih u MedDRA-i
HALMED na temelju članka 41. Pravilnika o farmakovigilanciji (Narodne novine, br. 83/13.) objavljuje popis nuspojava koje se smatraju ozbiljnima, a nisu jednoznačno određene kriterijima ozbiljnosti sukladno Smjernici o dobroj farmakovigilancijskoj praksi Modul VI - (GVP Module VI - Collection, management and submission of reports of suspected adverse reactions to medicinal products) radi harmonizacije prijavljivanja ozbiljnosti pojedinih nuspojava.
Popis ozbiljnih nuspojava kodiranih u MedDRA-i odgovara "Important medical events" listi (IME) izdanoj od MSSO-a. Ove nuspojave svrstavaju se u kategoriju "medicinski značajnih ozbiljnih stanja". Nositelj odobrenja obvezan je nuspojave iz Republike Hrvatske koje se nalaze na ovom popisu voditi kao ozbiljne te ih sukladno tome prijaviti u EudraVigilance.
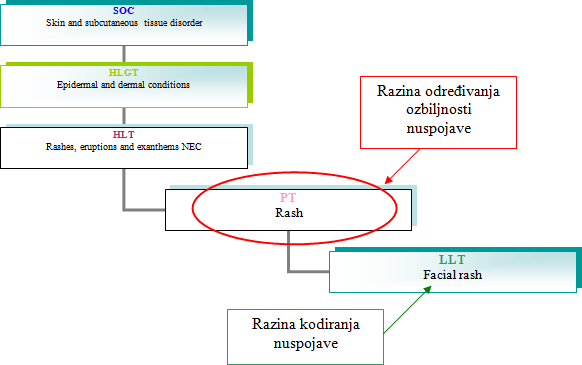
Popis se bazira na PT razini kodiranja u MedDRA-i koja se u većini slučajeva koristi za pretraživanja baze i u analizama. Nakon što se nuspojava kodira u LLT-u na temelju verbatima automatski mu se pridružuju nadređene kategorije. Ozbiljnost LLT-a treba provjeriti prema pridruženom PT-u. Primjer hijerarhije u MedDRA rječniku:
Lista ozbiljnih nuspojava / IME lista temeljena na ažuriranoj MedDRA verziji 29.0 (.xls)





