Podaci o zaprimljenim prijavama sumnji na nuspojave cjepiva protiv bolesti COVID-19
Cjepiva protiv bolesti COVID-19 se nakon odobrenja prate posebno intenzivno i s tim ciljem su na europskoj razini uvedeni mehanizmi pomoću kojih se regulatornim tijelima omogućuje da prikupe još više podataka o sigurnosti njihove primjene. Na nacionalnoj razini, u Republici Hrvatskoj prijave sumnji na nuspojave cjepiva zaprimaju i prate Agencija za lijekove i medicinske proizvode (HALMED) i Hrvatski zavod za javno zdravstvo (HZJZ). Zaprimljene prijave obrađuju se i ocjenjuju kao dio standardnog farmakovigilancijskog postupka.
Sve prijave koje HALMED zaprimi smatraju se sumnjama na nuspojavu te se koriste za kontinuiranu procjenu sigurnosnog profila cjepiva. Za svaku prijavu provodi se procjena povezanosti s primjenom cjepiva. Tek nakon temeljite ocjene svake prijave sumnje na nuspojave moguće je procijeniti je li povezanost između primjene pojedinog cjepiva i pojave pojedine nuspojave sigurna, vjerojatna, moguća, nije vjerojatna ili povezanost nije moguće ocijeniti. Ocijenjene prijave unose se u nacionalnu, europsku i svjetsku bazu nuspojava lijekova te čine dio dokumentacije o sigurnosti primjene cjepiva.
Cijepljenje u Republici Hrvatskoj trenutačno se provodi odobrenim cjepivima protiv bolesti COVID-19: Comirnaty (Pfizer/BioNTech); Spikevax, ranijeg naziva COVID-19 Vaccine Moderna (Moderna); Vaxzevria, ranijeg naziva COVID-19 Vaccine AstraZeneca (AstraZeneca, Sveučilište u Oxfordu); Jcovden, ranijeg naziva COVID-19 Vaccine Janssen (Janssen - Johnson & Johnson) i Nuvaxovid (Novavax). Informacije o predmetnim cjepivima možete pronaći ovdje.
Za svako odobreno cjepivo niže su navedene izravne poveznice na sažetak opisa svojstava lijeka (namijenjen zdravstvenim radnicima) i uputu o lijeku (namijenjenu pacijentima), koje sadrže sve informacije vezane uz sigurnu primjenu cjepiva, uključujući informacije o zabilježenim nuspojavama (dio 4. upute o lijeku, dio 4.8 sažetka):
- Cjepivo Comirnaty proizvođača BioNTech i Pfizer
- Cjepivo Spikevax proizvođača Moderna
- Cjepivo Vaxzevria proizvođača AstraZeneca
- Cjepivo Jcovden proizvođača Janssen
- Cjepivo Nuvaxovid proizvođača Novavax.
U nastavku su navedene informacije o broju prijava sumnji na nuspojave cjepiva protiv bolesti COVID-19 koje je HALMED zaprimio do sada. Tablica se ažurira svaki radni dan do 11 sati te uključuje sve prijave zaprimljene do 00:00 prethodnog dana.
| Ukupan broj prijava sumnji na nuspojave cjepiva |
|---|
| 6748 prijava |
|
3850 - Comirnaty, 798 - Spikevax (Moderna), 1701 - Vaxzevria (AstraZeneca), 387 - Jcovden (Janssen), 3 - Nuvaxovid (Novavax) i 9 prijava na COVID-19 cjepiva za koje nije zaprimljena informacija o proizvođaču
|
Izvor: HALMED, datum posljednjeg ažuriranja: 12. ožujka 2025. godine
Napominjemo da razlike u broju prijava sumnji na nuspojave ne upućuju na razlike u sigurnosti cjepiva. U Republici Hrvatskoj su zaključno s 31. prosinca 2022. godine primijenjene 5.354.084 doze cjepiva protiv bolesti COVID-19. Usporedbom broja prijava sumnji na nuspojave s brojem primijenjenih doza, dolazi se do zaključka da je na svakih 10.000 primijenjenih doza cjepiva zaprimljeno 12 prijava sumnji na nuspojave cjepiva. Drugim riječima, tek uz oko 0,12% primijenjenih doza cjepiva zabilježena je sumnja na nuspojavu. Udjeli prijava po broju primijenjenih doza po pojedinom cjepivu također su izrazito niski te se kreću u rasponu od 0,09% do 0,29%.
Napominjemo da je broj prijava sumnji na nuspojave općenito indikator kvalitete samog sustava prijavljivanja nuspojava. Ukazuje na visoku razinu osviještenosti zdravstvenih radnika i korisnika cjepiva o potrebi za prijavljivanjem nuspojava, čime se osiguravaju veće količine podataka koji služe za praćenje sigurnosnih profila cjepiva.
Temeljito prikupljanje i veća količina podataka o nuspojavama omogućuju bolji uvid u primjenu cjepiva te brzo uočavanje sigurnosnih signala zbog kojih bi eventualno bilo potrebno poduzeti odgovarajuće regulatorne akcije, kao što su primjerice nove preporuke, mjere opreza i slično. Također, iz navedenog prikupljanja i praćenja podataka proizlaze nove informacije za korisnike i zdravstvene radnike, što u konačnici dovodi do sigurnije primjene cjepiva.
Kakve su prijave zaprimljene?
Ozbiljnost nuspojava i uzročno-posljedičnu povezanost s cjepivom ocjenjuje Stručna grupa za nuspojave i sigurnu primjenu cjepiva HALMED-a i HZJZ-a. Ocjena, između ostalog, uključuje detaljan pregled svih dostavljenih informacija te nastavno prikupljanje dodatnih podataka od prijavitelja kada je to potrebno za provođenje cjelovitog postupka. Pritom se ocjena prioritetno provodi za prijave sumnji na ozbiljne nuspojave.
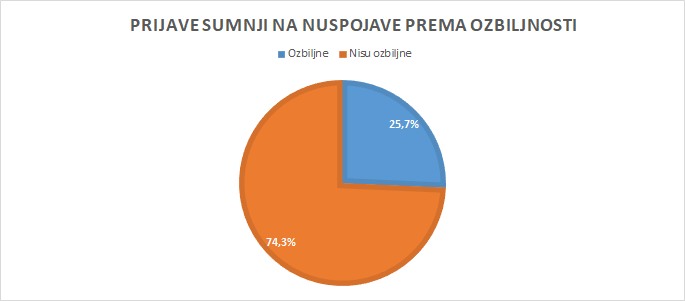
Među do sada zaprimljenim, ocijenjenim* te u europsku i svjetsku bazu nuspojava proslijeđenim prijavama sumnji na nuspojave, udio prijava koje nisu ozbiljne iznosi 74,3%, dok je 25,7% prijava ocijenjeno ozbiljnima.
* Budući da se ocjena prioritetno provodi za prijave sumnji na ozbiljne nuspojave, veći broj prijava koje nisu ozbiljne bit će uključen u sljedeće izvještaje.
Najčešće prijavljene nuspojave odnosile su se na povišenu tjelesnu temperaturu, bol na mjestu primjene, glavobolju, bol u mišićima, zimicu, opću slabost, umor, crvenilo na mjestu primjene cjepiva, mučninu i bol u zglobovima. Riječ je o očekivanim nuspojavama, koje se često javljaju, slične su nuspojavama drugih cjepiva te su najčešće blagog do umjerenog intenziteta i prolaze spontano kroz nekoliko dana ili uz primjenu simptomatske terapije (primjerice, hladni oblozi, lijekovi sa snižavanje povišene tjelesne temperature i lijekovi protiv bolova).
Pojedina prijava može sadržavati više nuspojava (kod pojedine osobe može se, primjerice, javiti glavobolja, povišena temperatura i bol na mjestu primjene cjepiva). Prikaz najčešćih nuspojava prema njihovoj zastupljenosti u zaprimljenim prijavama koje su unesene u svjetsku bazu VigiBase naveden je u nastavku.
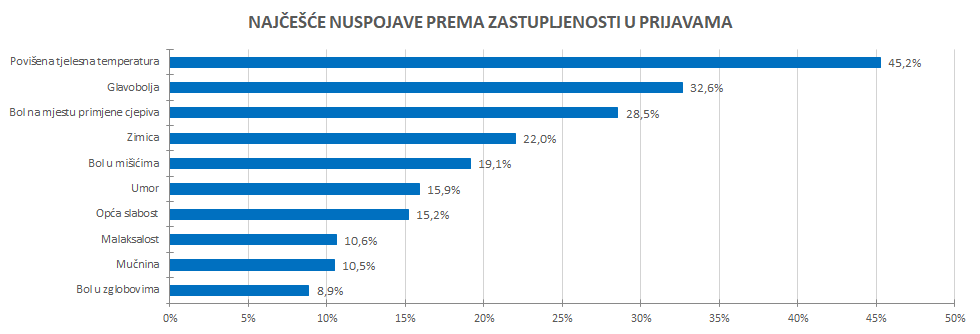
Izvor: Svjetska baza nuspojava VigiBase, 23. siječnja 2023. godine
Među ozbiljnim nuspojavama najčešće su zabilježene reakcije preosjetljivosti koje su se manifestirale kao osip, svrbež i koprivnjača nedugo nakon primjene cjepiva, u pojedinim slučajevima praćeno oticanjem lica, grla ili jezika te poteškoćama s disanjem ili gutanjem, zbog čega su primijenjeni antialergijski lijekovi i nakon čega je u svim slučajevima došlo do oporavka. Također, rjeđe su zabilježene reakcije pareze lica odnosno periferne slabosti jedne strane lica. Ove reakcije obično su povezane s otokom tkiva koji pritišće živac i najčešće je riječ o prolaznom stanju. Osim toga, zabilježeni su opsežno oticanje na mjestu primjene cjepiva, odnosno opsežna lokalna reakcija, visoka temperatura, tromboembolijski događaji te nesvjestice.
HALMED je do sada zaprimio ukupno 60 prijava sumnji na nuspojave sa smrtnim ishodom. Za jednu prijavu je slijedom provedene ocjene uzročno-posljedična povezanost s primjenom cjepiva ocijenjena kao vjerojatna. Za jednu prijavu je uzročno-posljedična povezanost ocijenjena kao moguća. Za 20 prijava je slijedom provedene ocjene uzročno-posljedična povezanost između primjene cjepiva i smrtnog ishoda ocijenjena kao: nije vjerojatna.
Za 38 prijava uzročno-posljedičnu povezanost s cijepljenjem iz trenutačno dostupnih podataka nije moguće ocijeniti. Za sve navedene prijave zatražena je dodatna medicinska dokumentacija, koja nije dostavljena uz inicijalnu prijavu a nužna je za provođenje ocjene. Od navedenih prijava, za 22 trenutačno nije zaprimljena zatražena dokumentacija, zbog čega nije moguće ocijeniti povezanost. Za 16 preostalih prijava dostavljena dostupna medicinska dokumentacija nije bila dostatna ili je zaprimljen odgovor da dokumentacija nije dostupna, stoga su navedene prijave ocijenjene stupnjem povezanosti nije moguće ocijeniti. U slučaju zaprimanja novih podataka, ponovno će se provesti ocjena uzročno-posljedične povezanosti.
Zaprimljeno je 9 prijava neželjenih događaja* sa smrtnim ishodom koje su vremenski povezane s razdobljem cijepljenja, no nisu uzročno-posljedično povezane s primjenom cjepiva.
Zaprimljeno je 16 prijava medikacijske pogreške, odnosno pogrešne primjene cjepiva, nakon kojih u 14 prijava nije došlo do nastanka nuspojava, dok je u 2 prijave zabilježena nuspojava.
Podaci o neželjenim događajima i medikacijskim pogreškama zanavljaju se nakon provedene zajedničke ocjene HALMED-a i HZJZ-a.
*U slučaju kada je događaj povezan s primjenom cjepiva isključivo vremenski no ne i uzročno-posljedično, riječ je o tzv. neželjenom događaju (ne o nuspojavi), koje su zdravstveni radnici također obvezni prijavljivati.
HALMED će nastaviti pratiti, prikupljati i ocjenjivati sve informacije vezane uz sigurnost primjene cjepiva protiv bolesti COVID-19 u Republici Hrvatskoj, kao i u drugim državama, te će redovito izvještavati o svim novim saznanjima.
Kako prijaviti sumnju na nuspojavu?
Sumnje na nuspojave mogu se prijaviti HALMED-u putem on-line obrasca, mobilnog uređaja ili slanjem obrasca. Osim toga, zdravstvenim radnicima je odnedavno omogućeno prijavljivanje sumnji na nuspojave putem elektroničke platforme OPeN, o čemu su dodatne informacije dostupne ovdje. Detaljnije informacije o postupku prijave sumnji na nuspojave dostupne su ovdje.
Dodatne informacije o ocjeni nuspojava
Više informacija o postupku ocjene prijava sumnji na nuspojave možete pronaći ovdje, a informacije o praćenju sigurnosti primjene lijekova dostupne su ovdje.





